Celler kontrollerar sine prosessar ut frå endringar dei registrerer i sitt miljø. Dette gjeld som oftast endringar i signalstoff som blir skild ut av andre celler. Signalstoff kan vera vekstfaktorar, hormon eller som i nervesystemet, neurotransmitterer. Det er kjemiske sambindingar nerveceller brukar for å kommunisere. Slik kommunikasjon skjer ved at proteinmolekyl på overflata av cella gjenkjenner spesifikt desse kjemiske strukturane og set i gang signalprosessane inne i cella. Denne prosessen bli utført av kompliserte maskineri av protein som påverkar kvarandre i spesielle mønstre. Desse gruppene av protein som verkar saman kallar vi signalvegar. I kompliserte organismar har mange signalvegar utvikla seg for at celler skal kunne snakke saman, gjerne fleire om gangen. Då er det viktig at dei forstår kvarandre! I fleire sjukdomstilstander er det nettopp dette som går galt.
Mykje av signaloverføringa i celler skjer ved ei kjemisk modifisering av proteina kor ei fosfatgruppe blir kopla på. Dette kallast fosforylering og gjev endra eigenskapar til proteina. For protein som er enzym kan det gje ei aktivering, for transkripsjonsfaktorer kan fosforyleringa gje auka binding til DNA og avskrift av gener. I mange tilfelle må spesielle protein kjenna att fosforyleringa og binde det modifiserte proteinet for at signalet skal ha effekt.
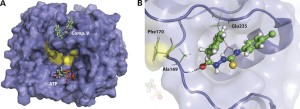
Vi har nyleg publisert resultat av eit arbeid kor vi har studert slik fosforylerings-styrt protein-protein binding. Vi brukte matematiske modellar for å undersøke korleis fleire ulike signalvegar kan styre regulering av sine målprotein ved help av slike protein-protein interaksjonar. I studien fokuserte vi på ein familie protein som nettopp har ei slik rolle i cella – 14-3-3 proteina. Dette er protein som det er spesielt mykje av i hjernen og som regulerer signalprosessar der.
Resultata viste korleis signalprosessar som påverkar kvarandre positivt eller negativt ved hjelp av 14-3-3 protein kan bli råka i ulik grad t.d. ved sjukdom kor signalstyrken er endra eller kor bindingskreftene mellom proteina er endra ved mutasjonar. Vi undersøkte også måtar ein kan retta opp att ei slik ubalanse.
Rune Kleppe (forskar)
Artikkelen: